 LA RADIOACTIVITÉ
LA RADIOACTIVITÉ 
1 - Historique et quelques définitions
2 - La radioactivité, une panacée
3 - Les dérivés de la radioactivité
1- Historique et quelques définitions
En décembre 1895, le physicien allemand Wilhelm Röntgen met en évidence la présence de rayonnements invisibles et pénétrants. Ils seront appelés tout d'abord rayonnements Röntgen ou Roentgen puis rayons X. À la suite de cette découverte, le physicien français Henri Béquerel veut vérifier si la phosphorescence de certains matériaux induite par les rayons X est la même que celle qu'on observe avec les minerais d'uranium. Il fait alors une découverte, presque par hasard. Elle commence avec des sels d'uranium qu'il oublie quelques jours sur une plaque photographique entourée d'un papier noir, le tout étant placé dans un tiroir fermé. En développant la plaque, il constate qu’elle a été impressionnée. Il fait d’autres expériences et conclut que certains sels d'uranium émettent des rayonnements pénétrants et invisibles mais différents des rayons X. Il vient de découvrir la radioactivité par ses propriétés ionisantes. L’appellation « rayons de Becquerel » est adoptée. Elle n’a pas été conservée car on a découvert plus tard qu’il y avait de trois rayonnements distincts.
En 1898, Pierre Curie et son épouse Marie Slodowsdka[1], d’origine polonaise, entreprennent de nouvelles recherches sur les rayonnements de Becquerel pour savoir si d'autres substances présentent cette étonnante propriété.
En juillet 1898, ils mettent en évidence une nouvelle substance radioactive, élément qu’ils baptisent polonium en l'honneur du pays d'origine de Marie.
En décembre 1898, ils découvrent encore un nouvel élément chimique, un million de fois plus radioactif, le radium, qui est présent dans un résidu de traitement de la pechblende, un des minerais d’uranium. Le radium possède des propriétés remarquables : il dégage spontanément de la chaleur, il est luminescent : la luminosité émise par une petite quantité (bien en-dessous du gramme) de radium permet de lire dans l'obscurité. Mis en présence de verre voire de diamant, il les « fume », les rendant presque opaques.
Marie Curie invente, à partir du mot radius, rayon en latin, le terme « radioactivité » qui qualifie la propriété d'émettre des rayonnements analogues à ceux de l'uranium.
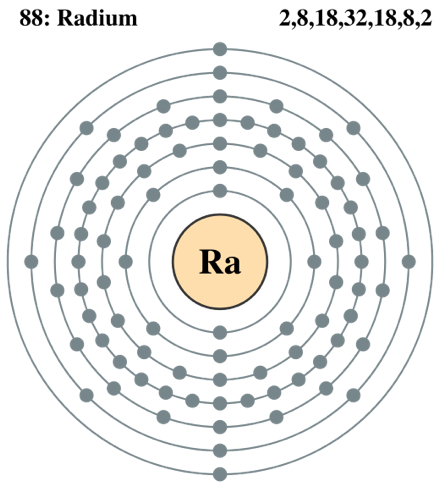
Image : L’atome de 22688Ra dans le modèle de Bohr. Il compte 226 protons et neutrons (nombre de masse, en exposant) dans son noyau et 88 électrons (numéro atomique, en indice) répartis sur 7 orbites : 2 électrons sur la plus externe, 8 sur la suivante, 18 sur la troisième etc.
[1] Marie Curie est une des rares personnes et la seule femme à avoir obtenu deux fois le prix Nobel, physique en 1903 et chimie en 1911.
Isotope
Chaque élément chimique est caractérisé par son atome. Malgré ce nom d’origine grecque qui signifie indivisible, insécable, l’atome est composé de particules plus petites : électrons, protons et neutrons. Ces deux derniers composent le noyau qui est entouré d’un nuage d’électrons, en nombre égal à celui des protons. Ce nombre est appelé numéro atomique, il définit l’élément, son nom et sa position dans le tableau de Mendéléef. Le numéro atomique, qui est égal au nombre de neutrons et de protons donne le nombre de masse qui caractérise le noyau. Le nombre de neutrons varie pour un élément donné ce qui revient à une variation du nombre de masse pour un numéro atomique donné. Chaque noyau définit un isotope de l’élément.
Sur un graphe représentant le nombre de masse en fonction du numéro atomique, on voit que les éléments sont disposés pratiquement le long d'une droite telle que les protons sont à peu près deux fois plus nombreux que les neutrons. Ceci laisse à penser que la stabilité de chaque élément et de ses éventuels isotopes dépend de ce rapport et donc qu'il ne peut rien exister loin de la droite.
Il s'avère que, même dans la zone « stable » entourant cette droite, des noyaux peuvent spontanément se décomposer sous l’effet d’une « oscillation quantique aléatoire », le Deus ex machina de la physique moderne. Lorsque l’énergie de l’oscillation quantique exigée pour la décomposition est relativement faible, l’isotope est instable, autrement dit « radioactif » car en se décomposant il émet des rayonnements. On parle alors de « radioisotope » ou de « radionucléide ». Les résidus de décomposition sont parfois eux-mêmes radioactifs, et constituent une chaîne de décomposition bien caractérisée.

Période
Les oscillations quantiques sont totalement aléatoires. Comme notre observation se fait à l’échelle d’un très grand nombre d’atomes, on est en droit d’établir des statistiques qui permettent de définir un certain nombre de paramètres, en particulier, celui de période.
Par définition, au bout d’une période, la moitié du matériau originel a été décomposée. Au cours d’une seconde période il en sera de même et ainsi il ne restera que le quart de l’original. Au bout d’une troisième période, seule la huitième partie subsiste et ainsi de suite selon les puissances inverses de 2. On parle de décroissance exponentielle. Après 10 périodes, il en subsiste moins du millième (exactement 1/1024 = 2-10)
Il convient de préférer le terme de période à celui de demi-vie qui conduit à croire qu’au bout de 2 demi-vies l’intégralité de la matière d’origine a disparu ce qui est faux, il en reste un quart. Cette erreur commune est entretenue par attirance sémantique. Exemple : la demi-heure est une moitié d’heure alors que la demi-vie n'est pas la moitié de la vie mais la perte de la moitié de la substance.
|
Elément |
Période |
|
Fer 56 |
Incommensurable |
|
Uranium 238 |
4,5 milliards années |
|
Potassium 40 |
1,25 milliard d'années |
|
Plutonium 239 |
24 000 ans |
|
Carbone 14 |
5 730 ans |
|
Radium 226 |
1 600 ans |
|
Américium 241 |
432 ans |
|
Césium 137 |
30 ans |
|
Strontium 90 |
28 ans |
|
Tritium 3 |
12 ans |
|
Cobalt 60 |
5 ans |
|
Iode 131 |
8 jours |
|
Technétium 99m |
6 heures |
|
Lawrencium 252 |
0, 36 seconde |
Radioactivité
Plus un élément sera instable, plus vite il sera décomposé et plus sa radioactivité par unité de temps sera élevée. Pour les isotopes dits stables, les durées restent inobservables, elles car outrepassent toute mesure. Le fer 56Fe en est un exemple. Les isotopes dont la période va de plusieurs milliards de fois la durée de l’Univers à quelques années, sont dits métastables. Les autres sont dits instables, leur période pouvant être inférieure au milliardième de seconde.
Rayonnement
En se décomposant les noyaux instables émettent un rayonnement de particules qui relève de trois types : alpha (noyaux légers d’hélium arrêtés par une simple feuille de papier), bêta (électrons arrêtés par une feuille d’aluminium) et gamma (photons de grande énergie arrêtés par une forte épaisseur d’une matière très dense tels plomb ou béton baryté).
La notion d’arrêt est assez relative. Dire que le libre parcours d’un alpha dans l’air vaut une quinzaine de centimètres signifie qu’il en reste la moitié et qu’il faut 1,5 mètre soit dix fois plus pour réduire au millième. Le libre parcours obéit au même type de loi « exponentielle » que celle utilisée pour la période.
L’énergie et le type du rayonnement sont spécifiques du noyau et permettent éventuellement de l’identifier.
Les dangers de la radioactivité
À part une irradiation massive, le principal danger est d’ingérer ou respirer des particules radioactives solides, des poussières ou des gaz qui continueront à se désintégrer dans l’organisme et donc à l’irradier localement.
On considère que les alphas sont 1000 fois plus mutagènes que les bêtas ou les gammas. Ils sont vite arrêtés donc absorbés par l’air voire la peau et n’interagissent donc peu ou pas avec l’organisme interne sauf si l’émetteur d’alpha a été ingéré ou respiré.
Les interactions créent des mutations qui à plus ou moins longue échéance évoluent en cancer.
La médecine nucléaire injecte des substances intégrant des éléments radioactifs tels l’iode 131 ou le technétium 99 en imagerie médicale ou expose à des doses importantes en radiothérapie (avec des aiguilles de radium jadis et du colbalt 60 maintenant). Une question se pose en terme de rapport bénéfice/risque.
Il ne sera pas parlé ici d’accidents nucléaires, le sujet mérite un développement complet à lui seul.
Le radon
Ce gaz qu’on nommait émanation du radium avant d’en connaître les caractéristiques est aujourd’hui « diabolisé » à cause de sa dangerosité. Chimiquement c’est un gaz « rare » car sa couche électronique externe est complète avec huit électrons : ce qui le rend inerte, inapte à toute combinaison chimique (sauf avec le fluor) et donc exempt de toxicité chimique.
On connaît 35 isotopes du radon, tous se décomposent très rapidement en un autre élément solide. Seul le 222Rn est significatif car sa période est de 3,8 jours ce qui rend son inhalation probable. Outre les mines d’uranium et de charbon, une des principales sources de 222Rn est la décomposition du radium 226 dans la filiation de décomposition de l'uranium 238 lequel est contenu dans les roches granitiques et les dépôts secondaires d’uranium d’où il diffuse à travers le sol. La rapidité de la transformation du radon en polonium 218 permet aux météorologistes de distinguer l’air continental de l’air maritime, celui-ci ayant totalement perdu son radon.
Le danger de l’inhalation de radon dépend du temps qu’il reste dans les poumons, eu égard à sa quantité et à sa période de 3,8 jours, celle-ci à la fois suffisamment brève pour qu’il ait le temps de se décomposer dans les poumons et suffisamment longue pour qu’il s’en trouve dans l’atmosphère. Sa filiation comprend des éléments solides qui, fixés dans le corps, vont à leur tour se décomposer pour finir en plomb 206 stable après avoir émis un total de 4 alphas, les plus mutagènes, de 5 bêtas bien agressifs et des gammas.
Certains estiment que 10 % des cancers pulmonaires seraient imputables au radon. Les 90% restant sont dus essentiellement au tabac.
Fission, fusion
Pratiquement tout ce qui a été dit plus haut est relatif à la fission, c’est à dire la décomposition d’un atome lourd. En comparant la masse du produit originel et celle des sous-produits, on trouve un petit écart, une petite diminution, sur la cinquième ou la sixième décimale. Comme masse et énergie sont équivalents, e = mC2, merci Albert Einstein, il y a donc production d’énergie. Ce qui est intéressant. Réacteurs nucléaires et bombe A reposent sur ce principe.
Un petit écart existe aussi si l’on fusionne 2 atomes plus légers que le fer mais ce n’est pas spontané (sur Terre) car il faut des températures énormes (million de degrés) et des pressions en proportion. De telles conditions se rencontrent au centre du Soleil. On sait faire fusionner 2 atomes d’hydrogène dans la bombe H qui est amorcée par la réaction de fission d’une bombe A. La maîtrise de la fusion offrirait une source d’énergie inépuisable. D’où les recherches actuelles : ITER, Tokamak etc.
Les unités de mesure
La communauté scientifique avait honoré les Curie (Ci) en donnant leur nom à l'unité de mesure de la radioactivité correspondant au nombre de noyaux qui se désintègrent dans un gramme de radium par seconde.
Aujourd’hui, l’intensité d’une source de rayonnement ionisant est mesurée en becquerel (Bq), avec 1 becquerel = 1 coup/seconde = 27 x 10-12 Ci
1 curie (Ci) = 3,7 x 1010 becquerel ou 37 milliards de désintégrations par seconde. Le becquerel caractérise l’activité d’une source, il peut être calculé par unité de masse, de surface ou de volume.
D’anciennes unités comme le rutherford (Rd) étaient aussi utilisées. On a 1 Rd = 1 MBq.
L’effet des radiations sur les organismes vivants n’est pas évalué par le becquerel.
La dose absorbée par kilogramme et par unité de temps est mesurée en gray[1] (Gy), unité de mesure qui ne tient compte ni de la source ni de la matière irradiée.
La dose efficace est mesurée en sievert[2] Sv, (plus souvent millisievert, mSv) qui détermine les effets des rayonnements sur l’organisme en entier.
Le sievert est homogène au gray, tous deux équivalents au joule par kilogramme, leur différence tient à la notion de dose émise pour le gray et de dose reçue pour le sievert. Dans le nouveau système international [3], le gray remplace le rad (rd) tel que 1 Gy = 1 rad et le sievert remplace le rem, tel que 1 Sv = 100 rem.
Appareils de mesure
Les premières mesures historiques ont été faites à l’électromètre à feuille d’or. Les rayonnements ionisants provoquent la décharge de l’électromètre que l’on compense par des charges piézoélectriques issues de la déformation d’un quartz. La mesure se fait indirectement par celle de la pression exercée sur le quartz : les travaux antérieurs de Pierre Curie sur la piézoélectricité ont été d’une grande utilité pour les travaux du couple Curie.
Il existe maintenant d’autres méthodes de détection des particules ionisantes.
Dans l’obscurité, avec une forte loupe, en présence d’un peu de matière radioactive, on observe dans un cristal de blende (sulfure naturel de zinc) une scintillation, lueur fugitive créée par le passage d’une radiation. Cet appareil est le spinthariscope inventé par William Crookes en 1903. En remplaçant la blende par un gros cristal d’iodure de sodium NaI et l’œil par un photomultiplicateur, on construit le scintillateur des prospecteurs d’uranium ou des médecins de médecine nucléaire lesquels parlent de scintigraphie alors qu’ils devraient dire scintillographie. Le traitement du signal électrique issu du photomultiplicateur fournit le nombre d'événements et leur énergie.
Au centre d’un tube métallique rempli d’un gaz sous faible pression on dispose un fil que l’on soumet à une haute tension, insuffisante pour amorcer l’arc : c’est le tube de Geiger-Müller. Le passage d’un rayonnement ionisant va créer une zone conductrice qui permet à l’arc de s’amorcer et qu’un dispositif annexe coupera. On compte les amorçages, les « coups » mais on ne peut rien en déduire de l’énergie de la particule. On trouve très facilement sur le marché de tels compteurs, l’URSS en avait produit des millions à la suite de Tchernobyl.
Une ou plusieurs cameras (pour la vision 3D) observent un liquide proche de sa température d’ébullition (hydrogène liquide) par ailleurs soumis à un champ magnétique. Le passage d’une particule déclenche localement l'ébullition du liquide de la « chambre à bulles » ce qui visualise la trajectoire et permet de caractériser le rayonnement.
Dans une enceinte de gaz sous faible pression et dans un champ magnétique, on empile des nappes de fils parallèles que l’on porte à un fort potentiel, positif pour les nappes paires et négatif pour les impaires. Le rayonnement ionise le gaz localement tandis qu’on mesure le courant issu de chacun des fils. Un traitement informatique restitue la trajectoire d’où l’on déduit l’événement. Cette « chambre à fils », mise au point par Georges Charpak en 1968 a complètement remplacé la chambre à bulles.
[1] En l'honneur de Louis Harold Gray, radiobiologiste anglais.
[2] En hommage à Rolf Sievert, physicien suédois.
[3] Recommandations 2007 de la Commission Internationale de Protection Radiologique - www.icrp.org/docs. Publication CIPR 103, 2009












